EUDAMED
Medical Device Regulation (EU), MDR 2017/745
1. 유다메드 EUDAMED 개요
유럽 의료기기 규정(MDR 2017/745)에 따라 구축된 EUDAMED는 의료기기 관련 규제 정보를 중앙에서 관리하는 통합 플랫폼으로,
여러 개의 모듈로 구성되어 있습니다.
SMG는 이 중 핵심인 UDI 모듈에 대하여 M2M 방식의 자동 업로드 연동을 지원합니다.
이는 기존의 번거로운 수동 입력 방식에서 벗어나, 대량의 UDI-DI 데이터를 구조화된 XML 메시지 형태로 전송함으로써 신속하고
정확한 자동 등록 및 업데이트를 가능하게 합니다.

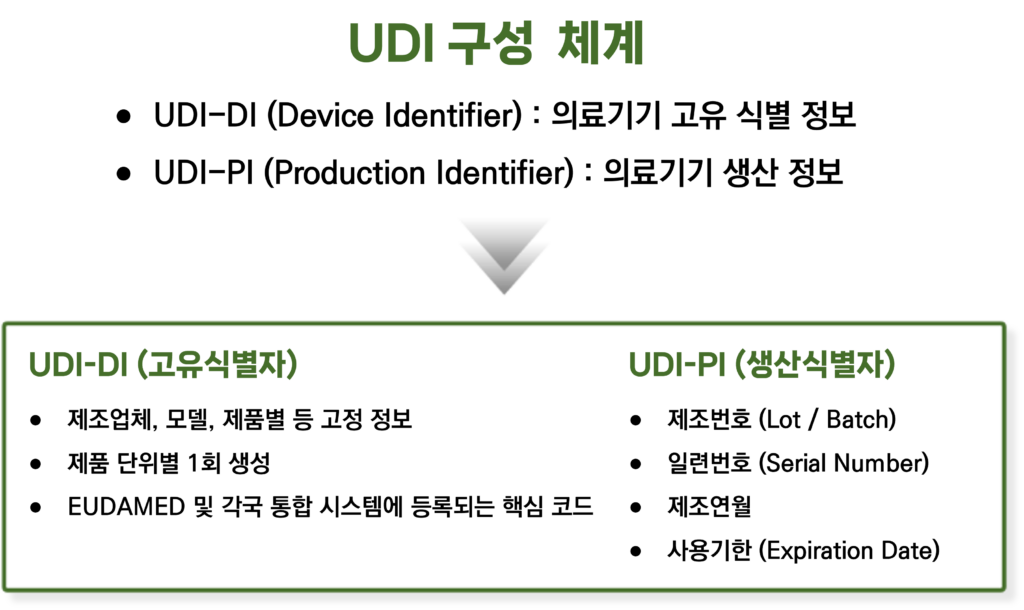
2. UDI 개요 (의료기기 표준코드_UDI)
UDI(Unique Device Identifier)는 의료기기를 식별 · 추적 · 관리하기 위한 국제 표준 식별 코드로, EUDAMED 내 UDI / 제품 등록 모듈을 통해 관리합니다.
즉, EUDAMED가 상위 플랫폼, UDI는 그 안에 포함된 핵심 데이터 체계입니다.
 ※표시의무
※표시의무
– 제조업자 · 수입업자는 모델명 / 포장단위별 UDI를 최소 포장단위 또는 최종 소비자 유통 단위에 바코드로 표시해야 함
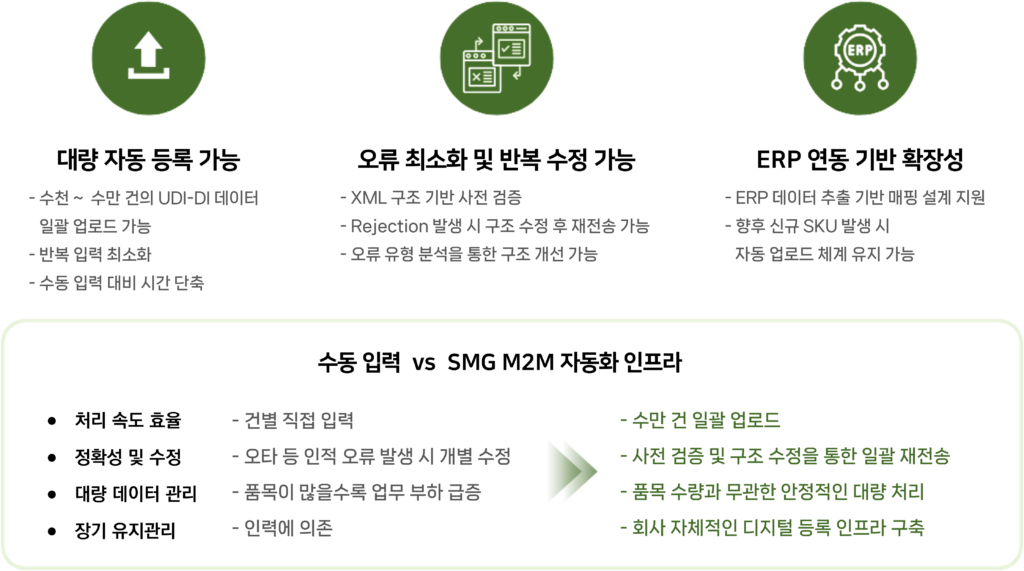
3. M2M 방식의 주요 특징
4. EUDAMED 의무화
EU 집행위원회 공식 결정
유럽 진행위원회(European Commission)가 공식 관보(OJEU)에 Commission Decision (EU)을 게재함에 따라, EUDAMED의 6개 모듈 중 준비가
완료된 4개 핵심 모듈이 ‘법적 의무 사용’ 상태로 선언되었습니다.
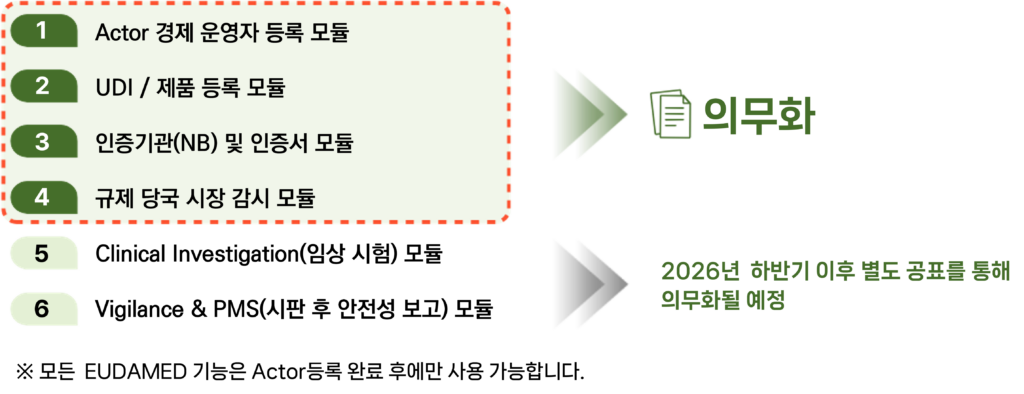
5. EUDAMED 의무화 주요 내용
법적 의무가 확정된 4가지 모듈의 주요 내용
- Actor Registration(경제 운영자 등록)
제조사, 유럽 대리인, 수입자 등이 EUDAMED를 사용하기 위해 시스템에 등록하고 **SRN(단일등록번호)**을 발급 받는 단계 입니다.
의무 : 모든 경제 운영자는 2026년 5월 28일까지 등록을 완료해야 합니다. - UDI / Device Registration(UDI 및 제품 등록)
의료기기의 고유 식별자(UDI-DI)와 제품의 특성 정보를 등록하는 과정입니다.
의무 : 신규 제품은 시장 출시 전 등록이 필수이며, 기존 제품은 별도 유예 기간 (2026년 11월까지) 내에 등록해야 합니다. - Notified Bodies & Certificates(인증기관 및 인증서)
유럽 인증기관(N/B)이 발행한 CE 인증서 정보를 시스템에 업로드하고 관리하는 모듈입니다.
의무 : 새로 발행된 인증서는 즉시 등록되어야 하며, 기존 인증서는 2027년 5월까지 등록 유예가 주어집니다. - Market Surveillance(규제 당국 시장 감시)
규제 당국이 유통 중인 의료기기의 안정성을 모니터링하고 필요한 조치를 기록하는 공적 감시 모듈입니다. ※ 공식 공표 이후 6개월의 전환 기간이 주어지며, 이후부터는 법적 강제성이 발생합니다.
※ 공식 공표 이후 6개월의 전환 기간이 주어지며, 이후부터는 법적 강제성이 발생합니다.
6. EUDAMED 진행 절차
- 안정성 : 복잡한 EUDAMED 구조를 직접 이해할 필요 없는 솔루션
- 효율성 : 수동 입력 부담 제로, 대량 제품 일괄 대응
- 전문성 : SMG를 통해 EUDAMED 자동 업로드까지 일괄 대응 가능

빠른 문의 하기